
伴随诊断试剂盒
伴随诊断(Companion Diagnostic ,CDx),对于其伴随药物的安全性及有效性非常重要,用于检测患者特定生物标志物,并识别出哪些患者能从药物治疗中明显获益或副作用风险增加。2014年,美国FDA首次明确定义了伴随诊断,此后日本PMDA、欧盟EMA相继发布了相关指南并定义了伴随诊断,中国NMPA在2020年发布的《已上市抗肿瘤药物的伴随诊断试剂临床试验指导原则(征求意见稿)》中也初步定义了伴随诊断。
伴随诊断的开发方法主要有同步(Co-development)、桥接(Bridging)、跟随(Follow-on)三种。FDA鼓励伴随诊断企业与药物研发企业密切合作,通过同步的方式可更经济地实现伴随诊断及其伴随药物的同时获批(Co- approval)。如果申请注册的伴随诊断(Candidate IVD Companion Diagnostic)与临床试验中用于主要疗效试验(Major Efficacy Trial)的临床试验检测(Clinical Trial Assay,CTA)不一样,FDA要求通过桥接研究的方式,分析原始临床试验样本来证明两种方法具有非常相似的性能特征。如果伴随诊断企业无药企合作伙伴或者最初临床试验中使用的样本无法获得,可使用跟随的方式。
迈杰转化医学作为国内精准诊断整体解决方案的领导者,拥有全技术平台及丰富的伴随诊断开发经验,可为药企合作伙伴提供伴随诊断一体化开发服务。公司围绕生物标志物研究、伴随诊断开发,建立了完善的核酸组学、蛋白组学、细胞组学技术平台。为创新药企开展全球多中心临床试验研究,提供中心实验室检测及伴随诊断开发服务,同时解决伴随诊断全球开发面临的问题。
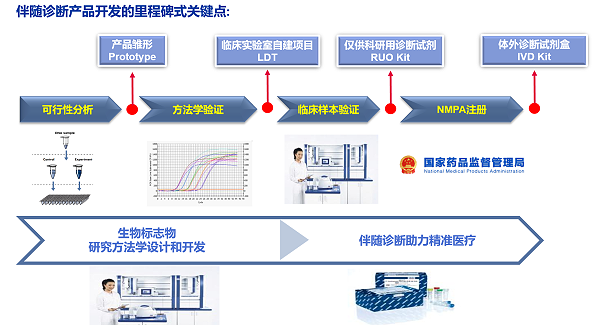
 创新诊断产品研发
创新诊断产品研发
● 迈杰转化医学的管理和技术研发团队,博士比例高于20%。
● 全组学平台专注药物伴随诊断研发及商业化,涵盖靶向治疗、免疫治疗和细胞治疗等产品。
● 已有多个诊断产品上市,多款产品进入临床试验阶段,同时还有多个肿瘤新药伴随诊断 产品进入研发管线。
 高标准质量体系
高标准质量体系
● 建立了覆盖全平台的产品研发实验室和质检实验室。
● 按照GMP和ISO 13485的要求建立覆盖全平台产品生产的生产车间。
● 研发实验室和生产车间已获的欧盟ISO 13485 认证证书,满足IVD/CDx产品设计 生产要求,通过NMPA 质量体系考核。